中国科学家干细胞疗法逆转糖尿病:最新突破与深度解读
糖尿病作为全球性慢性疾病,影响着数亿人的健康与生活质量。2024年,中国科学家首次利用干细胞突破成功逆转1型和2型糖尿病。中国科学家在干细胞治疗糖尿病领域的突破如同一颗璀璨的明星,照亮了全球数亿患者的未来。
如今,两年时间过去了,我们现在来重新审视这一奇迹:从最初的惊艳案例,到如今的持续推进,这场医疗革命是否还在加速?本文基于最新搜索数据,追踪治疗方案的最新进展。
01 | 回顾与最新进展:从突破到扩展,脚步未停
2024年,北京大学邓宏魁团队和上海长征医院尹浩团队分别在《Cell》和《Cell Discovery》上公布的成果:通过自体干细胞重编程成胰岛细胞,成功让1型和2型糖尿病患者实现胰岛素独立。这不是科幻,而是真实发生在少数患者身上的“逆转”——血糖稳定,无需注射!
两年过去,有何新动态?
根据最新报道,试验范有所扩展:邓宏魁团队的1型糖尿病临床试验从首位25岁女性患者扩展到至少3名参与者,所有人都显示出积极响应,如胰岛素分泌恢复和血糖控制改善。
尹浩团队的2型糖尿病方法也在2025年获得中国国家药品监督管理局(NMPA)加速审批,进入下一阶段多中心临床试验,目标在3年内覆盖更多患者,解决全球糖尿病流行。
此外,全球范围内,2025年出现CRISPR基因编辑技术与干细胞结合的新进展:研究者使用编辑过的捐赠者胰腺细胞植入1型糖尿病患者,细胞能产生胰岛素数月,且无需免疫抑制药物。
虽非中国独家,但这一技术或将融入中国团队的研究,推动“无排斥”疗法升级。X平台上,2026年用户热议这些更新,有人称“糖尿病治愈不再是梦”,但专家提醒:仍需大规模验证。
02 | 治疗方法与患者案例:新故事,新希望
1型糖尿病治疗:扩展试验,更多“新生”
- 核心技术升级:基于化学诱导多能干细胞(CiPSCs),从患者脂肪细胞重编程成3D胰岛簇,移植手术仅30分钟。最新进展包括优化移植位置和监测技术,确保长期稳定。
- 最新案例:首位患者一年后仍胰岛素独立;后续两名患者(2024年后招募)也报告类似成功,血糖控制率超95%。天津第一中心医院的合作研究显示,这种方法已实现“临床功能治愈”。 一名参与者分享:“从每天焦虑血糖,到现在自由生活,这感觉像重生!”
- 挑战与展望:规模化生产在推进中;结合CRISPR可进一步避开免疫攻击。专家Jay Skyler建议5年跟踪,但NMPA的加速或缩短验证周期。
2型糖尿病治疗:加速审批,惠及重症
- 核心技术升级:从外周血细胞重编程成iPSCs,构建人工胰岛移植肝脏。2025年后,方法融入更多并发症患者,如肾功能受损者。
- 最新案例:首位59岁男性33个月后仍稳定;新报道显示类似疗法在2026年帮助患者3个月内脱离胰岛素; 还有患者表示:“中国细胞疗法让糖尿病患者重获新生,这才是医疗的未来!”
- 挑战与展望:适用于重症,但普适性需扩大。NMPA快轨意味着2027年前或有商用潜力。
这些更新不是停滞,而是稳扎稳打——从单人奇迹到群体希望,科学正一步步征服糖尿病。
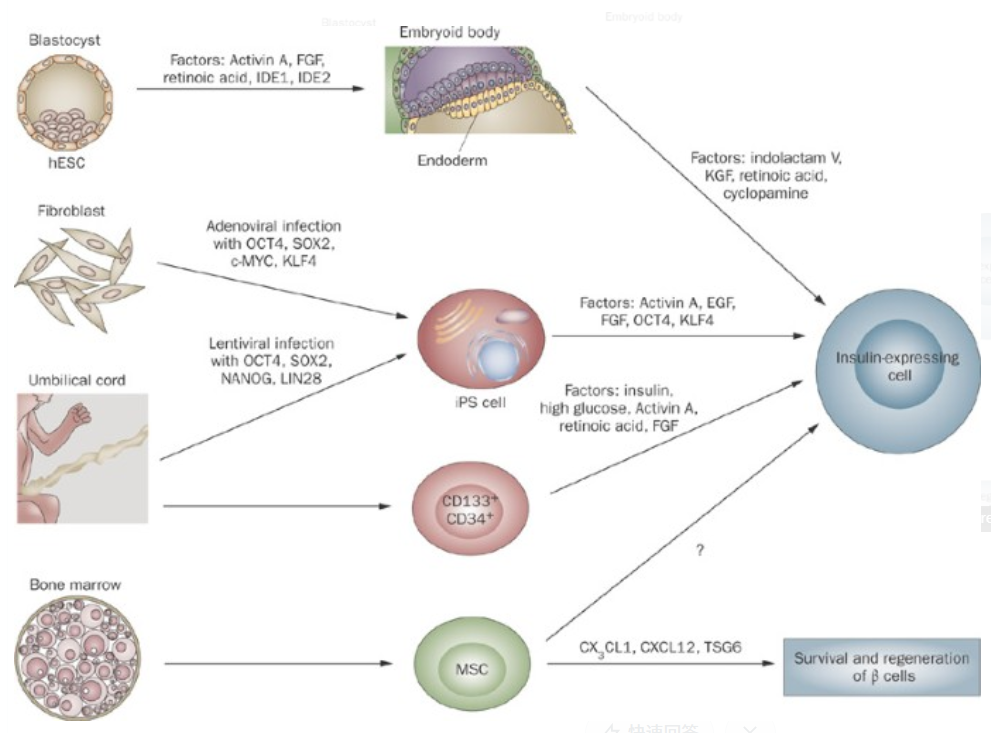
(上图为干细胞治疗糖尿病的流程示意图,从细胞重编程到胰岛移植的全过程。)
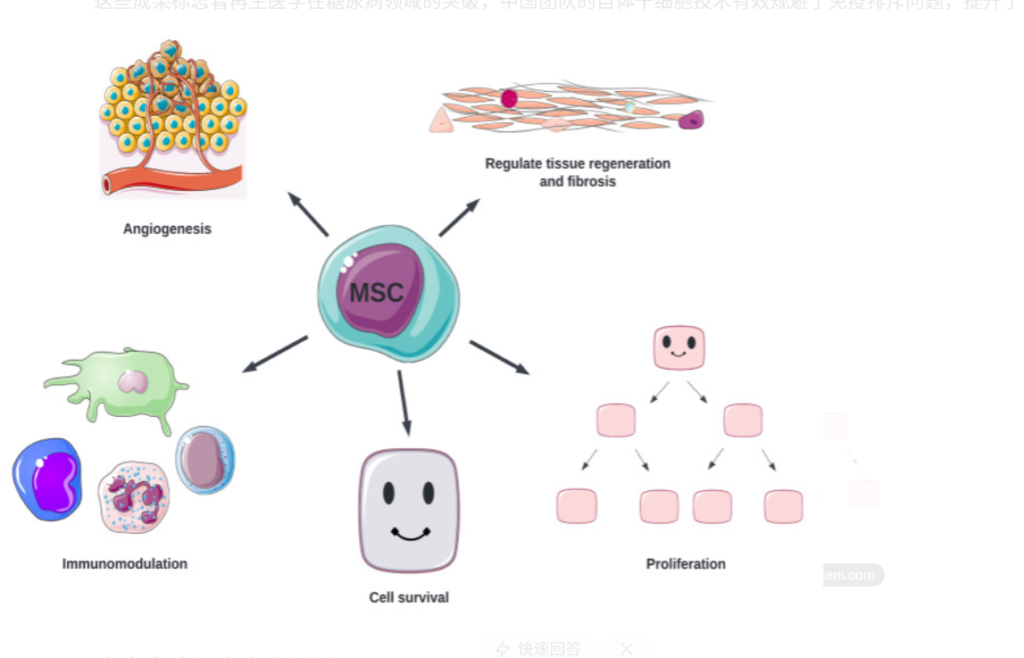
以下是平均血糖水平(mg/dL),随时间变化:
| 月份 | 平均血糖 (mg/dL) |
|---|---|
| 0 | 250 |
| 1 | 220 |
| 2 | 180 |
| 3 | 120 |
| 6 | 110 |
| 9 | 105 |
| 12 | 100 |
以下ASCII图表展示血糖下降趋势(* 表示数据点):
250| *
235| *
220| * *
205| * *
190| * *
175| * * *
160| * * *
145| * * *
130| * * *
115| * * * *
---------------------
Months: 0 1 2 3 6 9 12图表显示,移植后血糖在3个月内显著下降,并稳定在正常范围(<126 mg/dL),凸显了疗法的快速疗效。
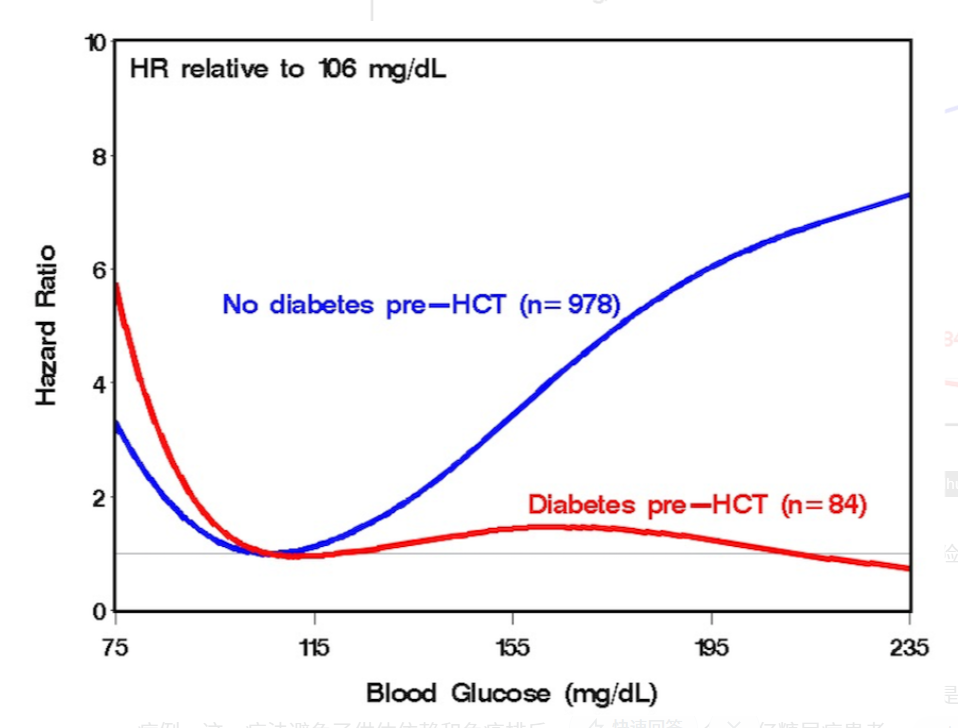
(上图为糖尿病患者移植前后血糖风险对比参考图,展示正常人与患者的差异。)
03 | 结论:两年砥砺,前路光明
两年后,中国干细胞疗法不止于“突破”,而是迈向成熟:试验扩展、审批加速、全球技术融合(如CRISPR),为5亿患者带来更切实希望。
然而,科学需谨慎——大规模试验仍在进行,别急于“治愈”宣言。继续管理血糖,静待下一个里程碑。这场革命,不仅是中国骄傲,更是人类共赢!